Une étude inédite sur les relations mammifères-virus
La cohabitation mammifères-virus a un long passé fait à la fois d’innocuité à l’endroit de ces pathogènes et d’épidémies dévastatrices, voire incontrôlables. De nos jours, eu égard l’expansion récente des populations humaines et de leurs animaux domestiques, les dangers de propagation de virus pathogènes sont un risque auquel l’Humanité est confrontée au quotidien, et qui ne peut que s’accroître dans l’avenir.
Est-il possible de se prémunir ou au moins de prévoir ces déferlantes virales qui risquent de nous décimer ?
Une approche probabiliste gérée par une Intelligence artificielle serait un premier pas pour nous garantir contre les virus inconnus qui nous menacent. L’équipe de Liverpool qui a conduit cette analyse a traité plus de 20 000 cas d’association entre des virus et des mammifères susceptibles d’en être les hôtes. Cette approche pourrait permettre de réduire d’un quart à un tiers le risque de contamination par des virus pathogènes 1.
L’intelligence artificielle développée par ce groupe de chercheurs dirigé par le Dr. M. Wardeh (Université de Liverpool) cherche à mémoriser et stocker les données actuelles connues sur les virus et leurs rapports avec les mammifères. Ces dernières sont ensuite traitées avec des algorithmes afin de cibler plus précisément et plus rapidement les couples virus-mammifères les plus à risque.
On estime que seulement 1 % des virus communs à tous les mammifères susceptibles un jour ou l’autre de nous agresser ont été identifiés. Pour notre plus grande chance, quelques-uns d’entre eux ont un pouvoir de propagation limité. Mais c’est une minorité : la plupart des virus, entre autres ceux de la rage et de la fièvre du Nil, sont présents chez presque tous les mammifères et peuvent provoquer à tout instant des épidémies de vaste échelle. Ce fut le cas des coronavirus, responsables des syndromes respiratoires SARS-CoV et MERS-CoV, dont les chauves-souris sont les hôtes et qui ont infecté les humains grâce à des intermédiaires : genettes, chameaux, mais aussi des chats, des furets et des pangolins.
Peut-on envisager de faire un inventaire exhaustif de tous les virus hôtes des mammifères et des zoonoses 2 qu’ils risquent de propager ? Certainement pas. D’autant que les décideurs ne sont guère disposés à financer ce type d’étude : voici quelques années, un projet avancé par une poignée de virologues américains n’a hélas été suivi d’aucun effet. Pourtant pour un coût raisonnable : avec 1,4 milliard de dollars sur trois ans, soit 75 fois moins que les dépenses engagées pour une seule année par la NASA, ces chercheurs se faisaient fort d’identifier et répertorier dans leurs moindres détails 380 000 virus, c’est-à-dire 85 % des virus pathogènes des mammifères. Ce fut un coup d’épée dans l’eau. Moins de dix ans plus tard, nous payons l’impéritie des responsables de cet aveuglement à l’endroit du risque épidémiologique qui menace au quotidien l’Humanité dans tous les pays, riches ou pauvres.
Sans doute les responsables d’alors ignoraient-ils ce fait historique premier, qui nonobstant devrait être enseigné dans toutes les écoles et se résume en ces deux images qui rendent compte de l’expansion exponentielle en terme de biomasse des populations humaines et de leurs animaux domestiques depuis dix mille ans :
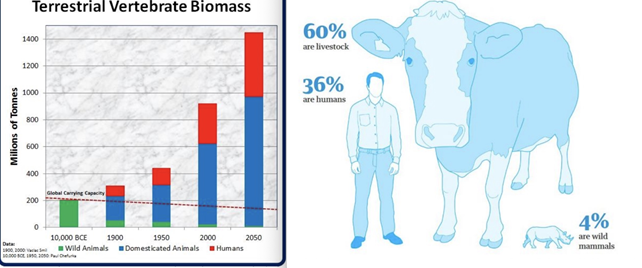
Dans une étude précédente, la même équipe ayant mis au point l’IA dont il est question dans cette recension a montré que le nombre d’hôtes possibles des coronavirus pathogènes chez les mammifères est plus élevé qu’estimé précédemment 3. La citation lapidaire qui résume leurs travaux d’alors énonce : « Il y a 40 fois plus d’espèces susceptibles d’être hôtes d’au moins quatre formes de coronavirus que ce qui était déjà connu, et environ 30 fois plus de mammifères chez qui pourraient se produire une recombinaison du Sars-CoV-2 susceptible de donner naissance à un nouveau virus pathogène ».
Au plan méthodologique, l’originalité de l’approche de ces chercheurs est qu’ils intègrent dans le spectre des critères traités par leur algorithme trois types de données :
- celles intrinsèques à chaque coronavirus de toute nature ;
- celles des hôtes potentiels qui peuvent les accueillir ;
- celles qui rendent compte du réseau coronavirus-hôte que l’expérience de terrain a pu mettre en évidence.
Sur ce sujet, le Dr Wardeh déclare : « Alors que les virus continuent de se déplacer à travers le monde, notre modèle offre un moyen puissant d’évaluer les hôtes potentiels qu’ils n’ont pas encore rencontrés. Cette prévision pourrait aider à reconnaître et atténuer les risques de zoonoses et de maladies animales, comme l’expansion des réservoirs de virus animaux susceptibles d’infecter les populations humaines. »
Son équipe élargit actuellement l’approche visant à prédire la capacité des tiques et des insectes à transmettre des virus aux mammifères à celle qui concerne les oiseaux, ce qui permettra de privilégier les études de laboratoire qu’il convient de mener. Cet élargissement des recherches aux oiseaux devrait accroître le potentiel de prédiction en relation avec l’écologie de virus dont on sait qu’ils sont les hôtes : virus de la fièvre du Nil, encéphalite du Japon et de nombreuses grippes.
Pour l’heure, ces chercheurs estiment que plus de 20 000 associations entre des virus connus et des espèces de mammifères restent à découvrir. La conclusion à tirer est que les connaissances actuelles sous-estiment le nombre d’associations virus-mammifères sauvages ou domestiques d’un facteur 4.3, et celui des virus pathogènes d’un facteur 3.2.
Autrement dit, il n’y pas que les chauves-souris et le pangolin dont nous devons nous préoccuper et nous méfier. L’illustrateur David Parkins a tiré les portraits de quelques-uns d’entre eux pour Nature 4. Pour mieux les combattre ne vaut-il pas mieux bien connaître ses faux amis ?

Jean-Louis Hartenberger
1. Maya Wardeh, Marcus S. C. Blagrove, Kieran J. Sharkey, Matthew Baylis. “Divide-and-conquer: machine-learning integrates mammalian and viral traits with network features to predict virus-mammal associations”. Nature Communications, 2021, 12.
2. Selon le Larousse [en ligne], une zoonose désigne une « maladie infectieuse atteignant les animaux, et qui peut être transmise à l’homme (peste, rage, etc.) ».
3. Wardeh, M., Baylis, M. & Blagrove, M. S. C. “Predicting mammalian hosts in which novel coronaviruses can be generated”. (2021) 12:780.
4. Smiriti Mallapathy, 2021. “The search for animal harbouring coronavirus – and why it matters”. Nature 591, 26-28.









